目前,第三批医疗器械唯一标识UDI实施工作正在有序推进,很多二类医疗器械企业也开始着手UDI的实施工作,咨询我们UDI的实施问题:“发码机构选哪个好?”“自己实施UDI行不行?”““想找第三方来实施,哪个比较靠谱?”
针对这些实施前期的高频问题,我们特意准备了这篇3000字的文章,希望能为大家带来一些帮助。
01 发码机构怎么选?
医疗器械生产企业实施UDI首先需要了解的是UDI发码机构和编码体系。
目前国家药监局认可三家发码机构,分别是中国物品编码中心(GS1 china)、中关村工信二维码技术研究院(ZIIOT)和阿里健康科技(中国)有限公司(阿里健康)。

上面的三家的码制都是符合要求的国药监要求的,但企业选择时需要结合产品的销售范围(有没有出口需求)、医疗器械使用单位的需求(在经销商端、医院能不能顺利扫码入库)、发码机构配套服务是否完善等因素来综合考虑。
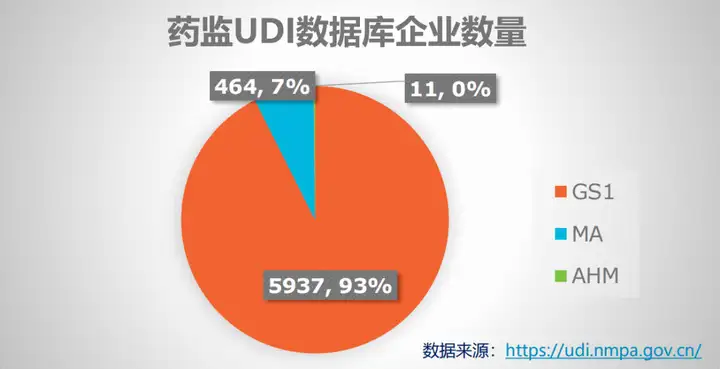
我们更推荐的发码机构是GS1,目前国家药监局数据库中,使用 GS1 标准的企业数量占比为93%,GS1的应用优势在以上三家发码机构中也非常明显,如:
GS1是唯一满足全球UDI要求的标准体系。目前,GS1标准是目前唯一同时满足多国法规的标准体系,可满足有出口需求的企业。
覆盖面广,供应链效率高。GS1标准覆盖150个国家和地区,被超250万家企业使用;国内选择GS1作为发码机构的医疗器械企业占比为93%,国内全行业GS1系统成员超520000家——各方采用同一套标准可以大大加快数据流通与应用的进程。
落地体系完善:全球有116个成员组织,国内设有47家物品编码分支机构,可以更好实地解决企业实际应用问题。
国家药监UDI示范单位全部使用GS1标准。国家药监局公布的首批15家首批医疗器械唯一标识实施示范单位名单中,7家生产企业、2家经营企业和6家医疗机构全部使用GS1标准。
02 企业自己来做UDI实施,会遇到哪些困难?
目前企业实施UDI一般有两种方式:
第一种是企业自行实施,企业指派专人或者组建实施专门团队,自行透彻学习UDI相关法规、熟知UDI实施流程和合规风险,找发码机构购买企业码段,然后根据发码机构提供的编码规则,自行完成UDI发码、编码、申报、赋码、数据管理、系统对接等工作。
第二种是企业找服务商完成UDI实施,例如慧铭科技-UDI服务平台作为中国物品编码中心的技术服务商和官方推荐服务商,就能提供UDI实施全流程服务,帮助企业精准高效完成合规相关工作。
两种方式都能完成UDI实施,但不建议企业自行实施,主要是以下方面原因:
1、自行实施UDI成本居高不下
如果企业自行实施,需组建专门的实施团队,实际案例中企业往往缺乏专业的医疗器械UDI实施人员和质量管理人员;而除了管理、实施、质量等部门参与外,还需组建软件开发团队,重新研发管理系统,自行进行产品编码,人力成本非常高。
而且,人力成本并非一次性投入,后期UDI的日常生产维护同样需要专人负责,人力成本需要持续支出。
2、实施基础薄弱,无法保证专业性和稳定性,隐性成本高
需指派专人花费较多时间学习和研究政策、法规。UDI学习成本高、合规难度高、复杂易错,整个实施过程不但需要不断摸索和试错,无法保证实施质量,如果企业主要负责UDI的员工岗位变动或者离职等,也会为接下来的工作带来较多问题。

3、编码合规性、系统安全性难以得到保障
一是编码合规性风险:不合规编码会造成标签浪费、甚至影响产品流通,如果产品本身编码复杂度就比较高,如IVD、义齿类,自行编码不合规的风险极大。另一方面,自行开发的编码系统安全性也难以得到保障。
4、UDI赋码问题
硬件能否正确采购,标签能否合规设计和打印,赋码方案能否适合产线都是企业需要考虑的问题。
5、数据管理难,潜在问题多
UDI是一个长期的生产运营体系,企业完成UDI实施后,还有持续性的运维工作。持续生产会让企业的UDI数据量不断增加。企业如果是选择自行实施,那么大量繁杂的数据需要专人管理,不仅存储、保管困难,还有数据管理不合规、数据丢失、后期追溯数据无法上传等潜在的安全问题难以解决。
此外,对于大部分企业来说,自行保管数据需要自建数据库,不仅需要相应的技术实力,这同样需要增加相应的成本预算。
6、政策变化风险
在适用的法规或标准发生变化时,企业如果敏感度不够,会有不符合法规要求或产品标准要求的风险。
UDI是医疗器械数据化的基础,UDI合规实施只是一个开始,是为今后的全行业追溯、“三医联动”等工作做准备,如果企业仅仅满足于完任务,而没有设计好底层框架,当后续法规出台之后,会导致企业出现更多的不可预知的问题,和后续成本和风险不可控。
所以,对于企业来说,自行实施UDI的性价比不高。
现在离第三批医疗器械唯一标识试点工作的截止日期已经不足十个月,加上不少省市已经加大UDI实施推进力度、越来越多医院开始要求入院产品有UDI码,对于企业而言,试错的时间已经没有多少了。
03 选择GS1官方标准服务,有哪些好处 ?
相比之下,选择GS1官方标准服务是一种高性价比的选择。通过规范的官方标准服务,比如UDI服务平台去完成UDI实施有哪些好处呢?

1、合规性强
官方标准的服务商对于编码规则的理解更为透彻,实施流程体系更为健全,对于整体实施工作的把控也更为成熟和健康。在这样的情况下,企业产品的合规性更高,能够更好避免产品不合规带来的种种不必要的风险。
2、数据安全框架更成熟
UDI数据与企业的生产和发展紧密相关,是关系着企业核心竞争力的重要数据。近年,企业数据安全事故频频发生,企业要能够安全存储、管理好这些数据,防止信息泄露。寻求专业的UDI标准服务商来搭建成熟的UDI数据安全框架是更经济高效的选择。
3、系统性强,长远指导更有效
UDI是一个系统性的体系,国家从生产端、流通端、使用端、发码机构、三医联动等多方面打造监管体系,目的是让医疗器械产品质量得到有效保障。企业未来要持续经营,就需要通过UDI体系对产品质量进行持续性的监管。
对于企业而言,UDI是一个长期性的动态过程,并不是一次性把编码完成然后上传就结束了。
在实施UDI时,企业应该具备系统思维,着眼于整体系统的搭建,而不是仅仅只看到UDI编码、赋码等过程。
同时,还要考虑到国家监管的发展方向,提前做出相应准备,这样,才能更好地确保UDI实施的合规性。
规范的官方标准服务能够精准把握政策和医疗行业发展特质,有前瞻性地指导企业如何实施UDI。
4、便捷性高,一站式服务更快捷
企业选择UDI服务平台后,只需要派出少量对接人员,即可高效率、安全、低损耗完成UDI的实施工作:
不需要聘请专业的医疗器械法规人员,或者自行摸索,全程由实施团队提供全部政策、法规培训,只需要指派对接人员,学习操作平台即可。 前中后期均有专家一对一指导,全程提供7*24小时服务与技术支持,全力保障企业按时按质完成UDI实施。 企业操作人员只负责了解平台功能和使用流程,其他工作全部由UDI服务平台智能管理,不需要担心人员不固定带来的损失。 不需要组建成本高昂的软件开发团队,在官方平台就可直接高效率完成编码、赋码和相关管理工作,且能自动完成合规校验。综上所述,对比了企业不同实施方案的优劣势之后,我们更加推荐企业直接选用GS1官方标准服务完成UDI实施,不仅省时省力、性价比高,而且合规安全更有保障。
慧铭科技-UDI服务平台是中国物品编码中心的指定技术服务商和官方推荐标准服务商,拥有15年医疗器械行业经验,公司核心团队多年行业深耕,精准把握医改政策和医疗行业发展特质。能够从长远的角度来指导企业如何实施UDI,为企业节省人力物力。
基于前期对UDI的深度理解和经验积淀,UDI服务平台可以为企业提供标准化和定制化的指导和服务,分行业、分类别的为企业提供适宜的解决方案。截至目前,UDI服务平台已协助2000多家医疗器械企业、200多家综合医院完成了UDI实施工作,并通过软件、标识、工业自动化等环节的合理配置,真正意义上实现了信息追溯、数据关联与共享。
在全球数字经济高速发展趋势下,UDI服务平台也将助力越来越多医械企业积极拥抱数字化,探索出更具前瞻性、能效更高、安全性更高、成本更低的管理路径,在市场竞争中获得更大的主动权,实现竞争力及企业价值的全方位提升。
免责声明:转载文章观点仅代表原作者本人,如有侵权请联系删除,我们将及时处理以保障双方权益。
 UDI服务平台-慧铭佳UDI-北京慧铭佳科技有限公司
UDI服务平台-慧铭佳UDI-北京慧铭佳科技有限公司 